在心血管疾病的临床诊疗中,一个令人困惑的现象时常出现:部分患者血压、血糖、血脂均控制在理想范围内,却仍突发心肌梗死。这一现象打破了传统认知中“三高”与心梗的简单因果关联,揭示出心血管疾病防治中更为复杂的病理机制。本文将从血管功能、炎症反应、凝血状态三个维度,探讨“三高正常却心梗”的深层原因。一、血管功能:从“结构正常”到“功能异常”的隐忧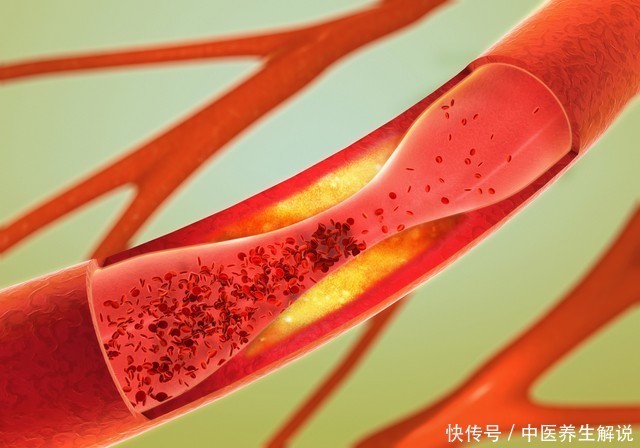 一氧化氮(NO)合成减少:内皮细胞受损后,NO合成酶活性下降,导致血管舒张功能减弱,局部血流灌注不足。氧化应激增强:内皮功能障碍时,超氧阴离子生成增加,与NO结合形成过氧亚硝酸盐,进一步削弱NO的生物活性。炎症因子释放:受损内皮细胞分泌黏附分子,促进单核细胞黏附并浸润血管壁,启动动脉粥样硬化进程。
一氧化氮(NO)合成减少:内皮细胞受损后,NO合成酶活性下降,导致血管舒张功能减弱,局部血流灌注不足。氧化应激增强:内皮功能障碍时,超氧阴离子生成增加,与NO结合形成过氧亚硝酸盐,进一步削弱NO的生物活性。炎症因子释放:受损内皮细胞分泌黏附分子,促进单核细胞黏附并浸润血管壁,启动动脉粥样硬化进程。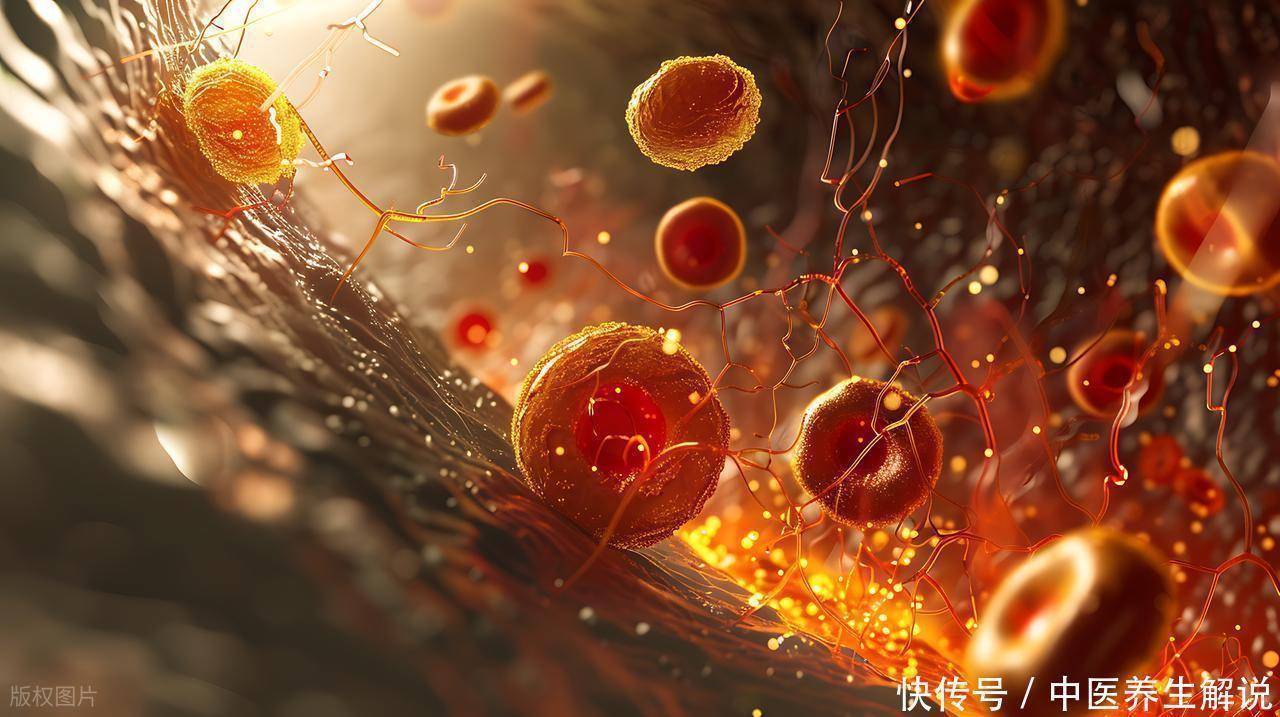 hs-CRP与斑块稳定性:hs-CRP升高可通过激活基质金属蛋白酶,降解斑块纤维帽的胶原成分,使斑块从“稳定”转为“易损”。炎症与内皮功能障碍:炎症因子(如IL-6、TNF-α)可抑制内皮细胞NO合成,同时促进血管平滑肌细胞增殖,加速动脉粥样硬化进程。炎症与凝血激活:炎症反应可上调组织因子表达,激活外源性凝血途径,增加血栓形成风险。
hs-CRP与斑块稳定性:hs-CRP升高可通过激活基质金属蛋白酶,降解斑块纤维帽的胶原成分,使斑块从“稳定”转为“易损”。炎症与内皮功能障碍:炎症因子(如IL-6、TNF-α)可抑制内皮细胞NO合成,同时促进血管平滑肌细胞增殖,加速动脉粥样硬化进程。炎症与凝血激活:炎症反应可上调组织因子表达,激活外源性凝血途径,增加血栓形成风险。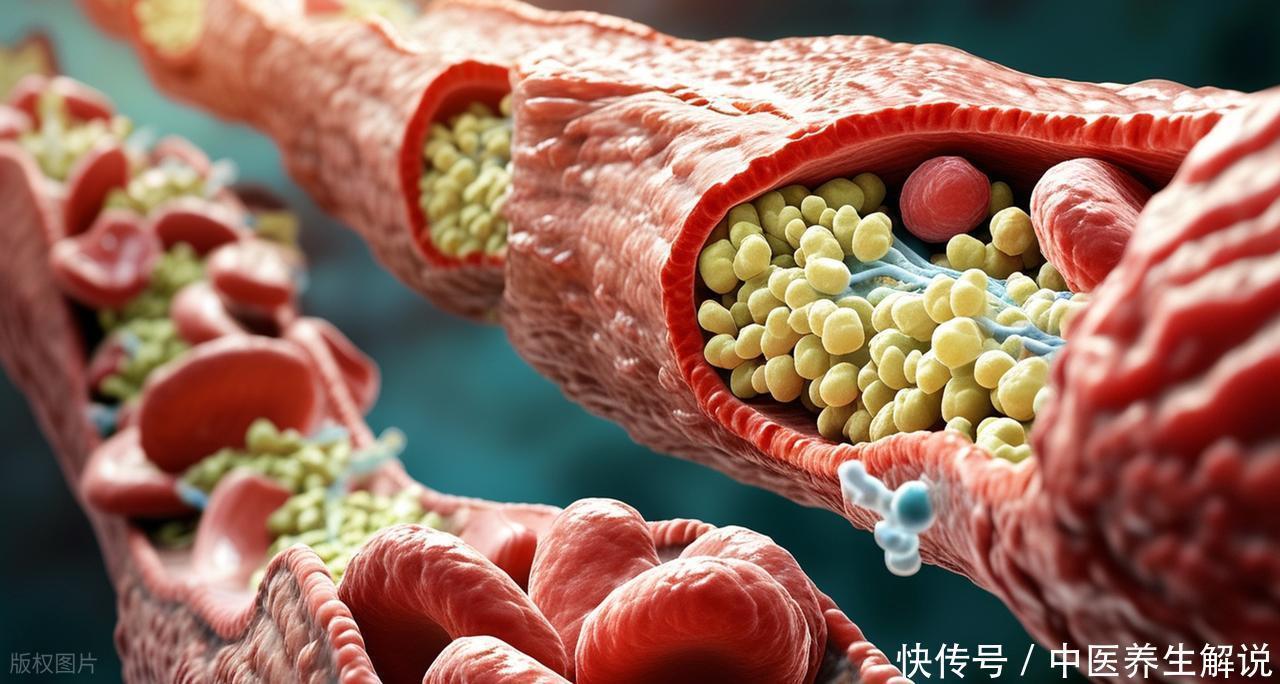 三、凝血状态:遗传与获得性因素的双重影响
三、凝血状态:遗传与获得性因素的双重影响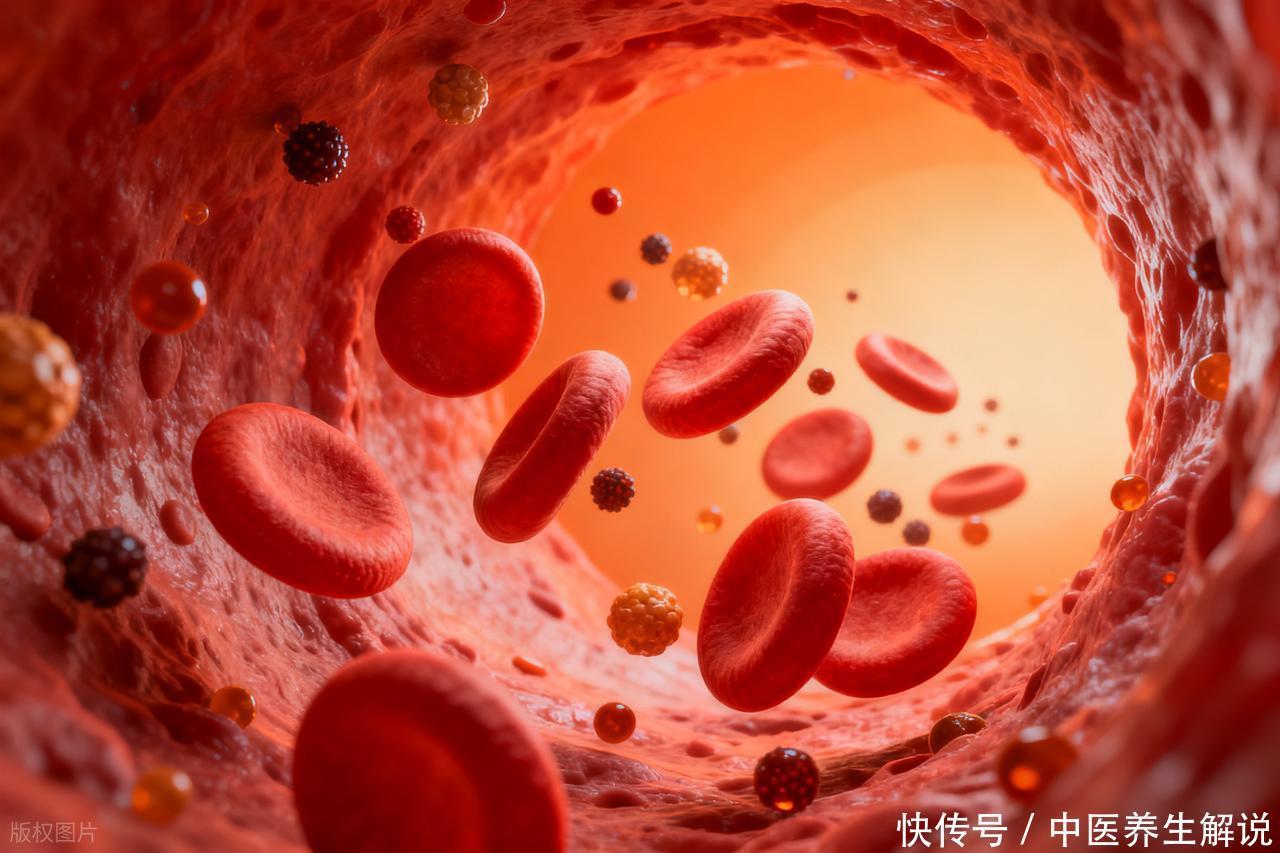
传统影像学检查(如冠脉CTA、冠脉造影)主要评估血管的解剖结构,却难以反映血管的动态功能。研究显示,约15%-20%的急性心梗患者冠脉狭窄程度<50%升富配资,其发病机制与血管内皮功能障碍密切相关。内皮细胞作为血管的“保护屏障”,其功能异常可通过以下途径诱发心梗:
 一氧化氮(NO)合成减少:内皮细胞受损后,NO合成酶活性下降,导致血管舒张功能减弱,局部血流灌注不足。氧化应激增强:内皮功能障碍时,超氧阴离子生成增加,与NO结合形成过氧亚硝酸盐,进一步削弱NO的生物活性。炎症因子释放:受损内皮细胞分泌黏附分子,促进单核细胞黏附并浸润血管壁,启动动脉粥样硬化进程。
一氧化氮(NO)合成减少:内皮细胞受损后,NO合成酶活性下降,导致血管舒张功能减弱,局部血流灌注不足。氧化应激增强:内皮功能障碍时,超氧阴离子生成增加,与NO结合形成过氧亚硝酸盐,进一步削弱NO的生物活性。炎症因子释放:受损内皮细胞分泌黏附分子,促进单核细胞黏附并浸润血管壁,启动动脉粥样硬化进程。这种“结构正常但功能异常”的状态,使得部分患者即使“三高”控制良好,仍因血管舒缩功能失衡或微循环障碍而突发心梗。
二、炎症反应:独立于“三高”的致病因素炎症在心血管疾病中的作用已得到广泛认可。高敏C反应蛋白(hs-CRP)作为全身炎症的敏感标志物升富配资,其预测价值独立于传统危险因素。研究显示:
 hs-CRP与斑块稳定性:hs-CRP升高可通过激活基质金属蛋白酶,降解斑块纤维帽的胶原成分,使斑块从“稳定”转为“易损”。炎症与内皮功能障碍:炎症因子(如IL-6、TNF-α)可抑制内皮细胞NO合成,同时促进血管平滑肌细胞增殖,加速动脉粥样硬化进程。炎症与凝血激活:炎症反应可上调组织因子表达,激活外源性凝血途径,增加血栓形成风险。
hs-CRP与斑块稳定性:hs-CRP升高可通过激活基质金属蛋白酶,降解斑块纤维帽的胶原成分,使斑块从“稳定”转为“易损”。炎症与内皮功能障碍:炎症因子(如IL-6、TNF-α)可抑制内皮细胞NO合成,同时促进血管平滑肌细胞增殖,加速动脉粥样硬化进程。炎症与凝血激活:炎症反应可上调组织因子表达,激活外源性凝血途径,增加血栓形成风险。一项纳入5000例受试者的队列研究显示,hs-CRP>3mg/L者5年心梗风险较hs-CRP<1mg/L者增加2.1倍,这一关联在“三高”控制良好的人群中依然显著。这提示我们:炎症指标的监测需与“三高”管理同等重要。
 三、凝血状态:遗传与获得性因素的双重影响
三、凝血状态:遗传与获得性因素的双重影响凝血功能的异常是心梗发病的独立危险因素升富配资,其机制包括:
遗传性凝血障碍:如抗磷脂抗体综合征、蛋白C/S缺乏症等,可导致高凝状态,即使“三高”正常,血栓风险仍显著升高。获得性凝血异常:如慢性肾病、恶性肿瘤、长期卧床等,可通过促进血小板活化或抑制纤溶系统,增加血栓形成风险。微血栓形成:在血管内皮功能障碍的基础上,凝血因子异常可导致微血管内血栓形成,引发心肌微循环障碍。研究显示,遗传性高凝状态者心梗风险较普通人群增加3-5倍,这一风险在“三高”控制良好的人群中并未降低。这提示我们:凝血功能筛查应纳入心梗高危人群的常规评估。

心脏不会因单一指标正常而停止跳动,心梗的防治也需跳出“三高”的框架。唯有以更立体的视角审视风险,从结构到功能、从代谢到炎症、从凝血到微循环升富配资,方能在无声的危机中守护生命。未来的心血管疾病管理,必将是一场融合多维度评估与个体化干预的精准之战。
龙辉配资提示:文章来自网络,不代表本站观点。
沪深京指数
热点资讯



